
Что такое церебральный дефицит фолатов
Фолаты — семейство из более чем 25 структурно родственных соединений, объединённых общим названием «витамин B9». Они необходимы для синтеза ДНК, деления клеток, производства нейромедиаторов и эпигенетического контроля экспрессии генов. Без достаточного количества фолатов в нервной системе нарушаются сразу несколько критических процессов: синтез дофамина и серотонина, метилирование ДНК, производство миелина и антиоксидантная защита.
В 2004 году группа исследователей во главе с Винсентом Рамакерсом ввела термин «церебральный дефицит фолатов» (Cerebral Folate Deficiency, CFD). Он описывает состояние, при котором уровень активной формы фолата — 5-метилтетрагидрофолата (MTHF) — снижен в спинномозговой жидкости, при этом концентрация фолата, витамина B12 и гомоцистеина в крови остаётся нормальной.
Это ключевой момент: стандартный анализ крови на фолат и B12 не выявляет церебральный дефицит. Мозг может голодать, пока кровь показывает норму.
Как фолат попадает в мозг
Основная циркулирующая форма фолата в плазме — 5-метилтетрагидрофолат (MTHF). Чтобы попасть в мозг, MTHF должен пройти через гематоэнцефалический барьер в области хориоидного сплетения. Этот транспорт обеспечивается двумя белками, работающими в паре:
- Фолатный рецептор альфа (FRα) — мембранный белок, закреплённый на поверхности клеток хориоидного сплетения через GPI-якорь. Он связывает MTHF и инициирует эндоцитоз — захват молекулы внутрь клетки в составе везикулы.
- Протон-сопряжённый переносчик фолатов (PCFT) — обеспечивает высвобождение фолата из эндосомы внутрь клетки.
После прохождения хориоидного сплетения MTHF попадает в спинномозговую жидкость, затем через эпендимальный барьер проникает в паренхиму мозга и включается в метаболизм нейронов.
Аналогичный FRα-опосредованный механизм транспорта работает на плацентарном барьере (доставка фолата к плоду), в гонадах (мужских и женских) и в щитовидной железе в пренатальном периоде и первые месяцы после рождения.
Пять механизмов церебрального дефицита фолатов
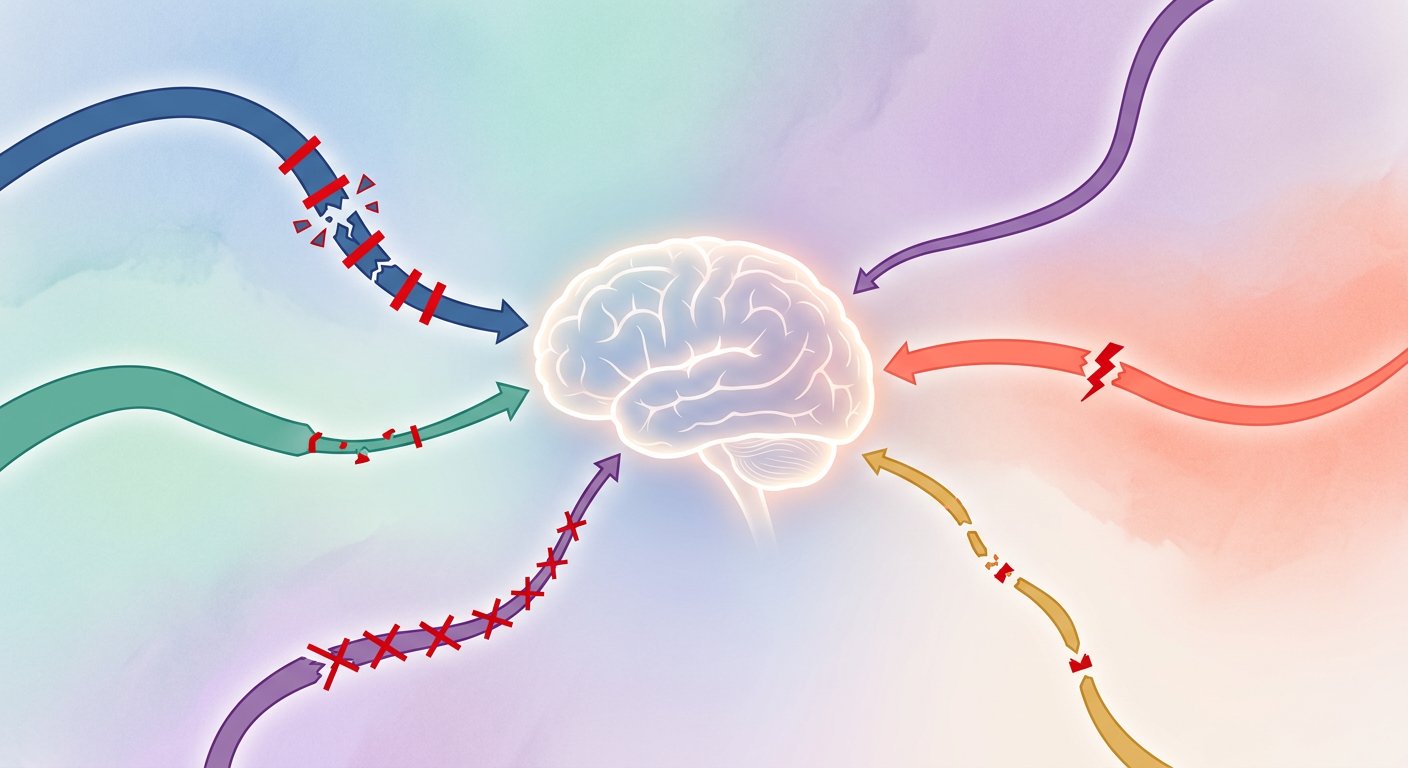
Согласно классификации Рамакерса и Квадроса, существует пять основных механизмов, приводящих к CFD:
I. Нарушение транспорта фолатов через гематоэнцефалический барьер. Сюда относятся: дисфункция FRα (аутоантитела, мутации гена FOLR1, нарушения сигнальных путей эндоцитоза, изменение состава мембран при синдроме Смита-Лемли-Опица), нарушения энергетического метаболизма (митохондриальные заболевания, дефицит GLUT1), а также повреждение хориоидного сплетения (кровоизлияния у недоношенных, инфекционные и иммунные поражения, окислительный стресс).
II. Истощение внутриклеточного запаса фолилполиглутаматов. Уменьшение депонированных форм фолата внутри нейронов.
III. Повышенное потребление фолатов в мозге. Наследственные дефициты ферментов (дефицит ароматической аминокислотной декарбоксилазы, дефицит дигидроптеридинредуктазы), ятрогенные причины (карбидопа при болезни Паркинсона), а также инфекционные и иммуноопосредованные процессы (подострый склерозирующий панэнцефалит, энцефалит Расмуссена).
IV. Повышенный катаболизм фолатов. Окислительный и нитрозативный стресс разрушают молекулы MTHF и повреждают транспортные белки. Дефицит антиоксидантных ферментов (глутатионпероксидаза, супероксиддисмутаза) и их кофакторов (селен, марганец, убихинон Q10) усугубляет ситуацию.
V. Нарушения фолатного метаболизма в мозге. Дефициты ферментов фолатного цикла (MTHFR, серин-гидроксиметилтрансфераза, дигидрофолатредуктаза), истощение пула одноуглеродных доноров (дефицит 3-фосфоглицератдегидрогеназы), гипергомоцистеинемия при сочетанном дефиците витаминов B2, B6, B9 и B12.
FRα-аутоантитела: главная причина
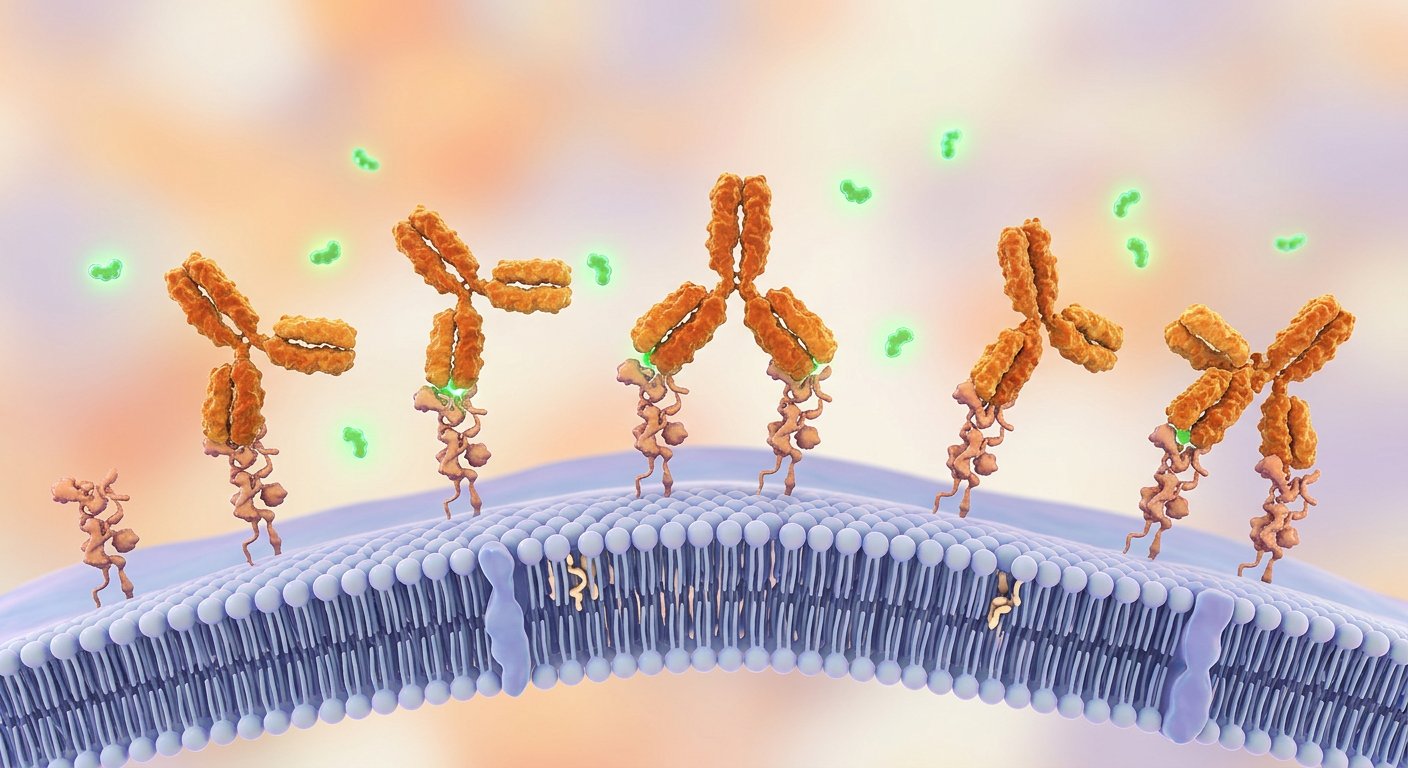
Наиболее распространённая причина CFD — аутоантитела к фолатному рецептору альфа (FRα). Выделяют два типа:
- Блокирующие антитела — связываются непосредственно с участком FRα, ответственным за захват фолата, и физически препятствуют связыванию MTHF.
- Связывающие антитела — присоединяются к FRα вдали от фолат-связывающего сайта, но активируют комплемент-опосредованное воспаление с последующим разрушением комплекса FRα-антитело.
Оба механизма приводят к одному результату — снижению общего транспорта фолата в мозг.
Откуда берутся эти антитела
Белок FRα человека имеет примерно 90% гомологии аминокислотной последовательности с FRα, присутствующим в молоке и молочных продуктах животного происхождения. У генетически предрасположенных людей поступление растворимого FRα из коровьего молока через кишечник стимулирует иммунную систему к выработке антител, которые перекрёстно реагируют с собственным FRα на хориоидном сплетении, щитовидной железе и гонадах.
Этот механизм подтверждается экспериментально: безмолочная диета (исключение молока и молочных продуктов животного происхождения) приводит к снижению титра FRα-антител в течение 3–6 месяцев, тогда как повторное введение молочных продуктов вызывает их повторный подъём.
Установлена обратная корреляция между титром FRα-антител и уровнем MTHF в спинномозговой жидкости. Ещё одна особенность: титры антител колеблются циклически с периодом 5–7 недель, поэтому единичный отрицательный результат не исключает диагноз.
Возрастной спектр клинических синдромов

Клиническая картина CFD определяется возрастом, в котором развивается дефицит фолата в мозге, а также наличием или отсутствием FRα-аутоиммунитета у родителей.
Инфантильный CFD (дебют в 4–6 месяцев)
Первое описанное и наиболее полно изученное состояние. Начальные симптомы — нарушения сна, беспокойство, ажитация у ребёнка 4–6 месяцев, которые нельзя объяснить гастроэзофагеальным рефлюксом или аллергией на молоко. В течение следующих двух лет формируется полная клиническая картина:
- Замедление роста окружности головы
- Психомоторная задержка, гипотония, атаксия
- Дистальные пирамидные знаки (при отсутствии лечения — прогрессия до тетраспастики)
- У трети пациентов — дискинезии (хореоатетоз, дистония) и/или эпилептические приступы
- Прогрессирующая потеря зрения с 3 лет, потеря слуха с 6 лет
При МРТ у половины нелеченых пациентов — задержка миелинизации, субкортикальная и перивентрикулярная демиелинизация, церебральная и церебеллярная атрофия. У меньшинства детей с инфантильным CFD развивается аутизм.
Аутизм с неврологическим дефицитом
У детей с низким IQ, аутизмом и типичными неврологическими признаками инфантильного CFD обнаруживаются столь же низкие уровни MTHF в спинномозговой жидкости и аналогичные титры FRα-антител, что и при «классическом» инфантильном CFD. Принципиальное отличие: у родителей детей с аутизмом FRα-антитела обнаруживаются у одного или обоих родителей, тогда как у родителей детей с инфантильным CFD без аутизма антитела отсутствуют.
Это указывает на то, что аутистические черты могут быть связаны с последствиями FRα-аутоиммунитета у родителей, влияющего на фолат-зависимые процессы в сперматозоидах, ооцитах и/или на внутриутробное развитие.
Инфантильный аутизм без неврологического дефицита
Дети с аутизмом без выраженных неврологических нарушений демонстрируют менее глубокое снижение MTHF в спинномозговой жидкости по сравнению с инфантильным CFD, но уровни статистически значимо ниже, чем у здоровых контролей. Титры FRα-антител сопоставимы с другими группами. У значительной доли родителей этих детей также обнаруживается FRα-аутоиммунитет.
Спастико-атактический синдром (1–2 года)
Появление FRα-антител у детей в возрасте 1–2 лет приводит к спастико-атактическому CFD-синдрому с нарушениями обучения.
СДВГ и поведенческие нарушения (2–5 лет)
У небольшой доли детей с синдромом дефицита внимания и гиперактивности, нарушениями обучения и поведенческими отклонениями в возрасте 2–5 лет обнаруживается FRα-аутоиммунитет. Неврологическое обследование выявляет лёгкую атаксию походки и положительную пробу Ромберга.
Шизофрения и психотические расстройства (подростки и взрослые)
FRα-аутоиммунитет может предрасполагать к тяжёлым психотическим эпизодам и рефрактерной шизофрении. В исследовании 20 пациентов с рефрактерной шизофренией FRα-антитела обнаружены в 85% случаев. Характерная особенность — выраженные колебания титра антител с периодом 5–7 недель, что может объяснять чередование позитивных и негативных симптомов.
Резистентная депрессия
У 9 из 16 обследованных пациентов (56%) с тяжёлой терапевтически резистентной большой депрессией обнаружены FRα-антитела. Терапия фолиновой кислотой демонстрирует определённую эффективность.
Дистония и паркинсонизм
Описаны спорадические случаи тяжёлой дистонии или паркинсонизма в сочетании с психиатрическими расстройствами, не реагирующими на стандартную терапию, при которых был выявлен CFD на фоне FRα-аутоиммунитета.
Деменция (взрослые)
Описан случай взрослой женщины с деменцией и миоклонусом, у которой был диагностирован CFD-синдром. Систематических исследований при разных формах деменции пока не проводилось.
Диагностический алгоритм
Диагностика CFD строится на клиническом подозрении с учётом возраста, анамнеза и неврологического статуса пациента.
Первая линия обследования
- Общий анализ крови, сывороточный и эритроцитарный фолат, витамин B12 в плазме, гомоцистеин, лактат, КФК
- Функция печени и почек, ТТГ, Т3, Т4
- Ферритин, медь, цинк, марганец, селен
- Общий холестерин, аполипопротеин B, коэнзим Q10
- Витамины A, B2, B6, C, D, E и гамма-токоферол
- Антитела к глиадину
- Генотипирование MTHFR (C677T и A1298C)
Ключевой тест
Определение FRα-аутоантител в сыворотке (блокирующего и связывающего типа). Важно: за 3 дня до тестирования следует прекратить приём добавок, содержащих фолаты. При отрицательном результате тестирование рекомендуется повторить через несколько недель из-за цикличности колебаний титра.
Для инфантильного CFD и аутизма люмбальная пункция не всегда обязательна — сначала определяется наличие FRα-антител в сыворотке, которые обратно коррелируют с уровнем MTHF в спинномозговой жидкости.
При отрицательных FRα-антителах
- Мутации гена FOLR1 и CIC
- Исключение митохондриальных дефектов
- Мутации MTHFR
- Маркёры окислительного стресса и уровни кофакторов антиоксидантных ферментов (железо, медь, цинк, селен, марганец)
- Люмбальная пункция для определения MTHF, птеринов, метаболитов моноаминов
При аутизме — обследование родителей
Если у ребёнка с аутизмом обнаружены FRα-антитела, рекомендуется определить наличие антител у обоих родителей — это влияет на прогноз лечения.
Фолиновая кислота
Основа терапии при CFD, вызванном FRα-аутоиммунитетом, — высокие фармакологические дозы фолиновой кислоты:
- dl-фолиновая кислота (dl-5-формилтетрагидрофолат): начальная доза 0,5–1 мг/кг/сут, при необходимости увеличение до 2 мг/кг/сут (максимум 50 мг/сут)
- Лево-фолиновая кислота: 0,25–0,50 мг/кг/сут
- Лево-5-метилтетрагидрофолат: эквивалентная доза (не одобрен для медицинского применения в Европе)
Критически важно: начинать лечение следует с половины целевой дозы в течение первого месяца. Резкое повышение фолата в мозге приводит к увеличению продукции тетрагидробиоптерина, дофамина и серотонина с последующей гиперстимуляцией синапсов. Для установления нового равновесия между выработкой нейромедиаторов и плотностью ранее подавленных рецепторов требуется около 6 недель. При выраженной ажитации или агрессии — временное назначение рисперидона в низкой дозе на 2–3 месяца.
При CFD, обусловленном мутациями FOLR1, необходимы более высокие дозы — до 5–7 мг/кг/сут — для компенсации функциональной потери рецептора.
Безмолочная диета
Исключение молока и молочных продуктов животного происхождения (замена на растительное молоко) устраняет экспозицию к растворимому FRα, запускающему перекрёстную иммунную реакцию. Титр FRα-антител снижается через 3–6 месяцев диеты. Диетические меры можно вводить сразу после забора диагностических образцов, не дожидаясь результатов.
Ограничение: дети с расстройствами аутистического спектра часто не принимают или не переносят столь строгую диету из-за пищевой избирательности.
Особые ситуации
Тяжёлые дискинезии, частые судороги, эпилептический статус: кортикостероиды для подавления FRα-аутоиммунитета до наступления терапевтического эффекта фолиновой кислоты.
Митохондриальные заболевания (болезнь Альперса, синдром Кернса-Сейра): фолиновая кислота с вариабельным ответом; добавление антиоксидантов может помочь, но убедительных доказательств значимого улучшения пока нет.
Мутации MTHFR (C677T гомозигота, C677T/A1298C компаунд-гетерозигота): часть дозы фолиновой кислоты целесообразно заменить эквивалентной дозой лево-метил-ТГФ, поскольку MTHF — единственная форма фолата, пересекающая гематоэнцефалический барьер. Высокие дозы рибофлавина необходимы для повышения активности MTHFR.
Дефицит витамина D: снижает экспрессию гена RFC1 (альтернативный путь транспорта фолата при высоких концентрациях). Коррекция дефицита витамина D обязательна при терапии CFD.
Нутритивные дефициты при аутизме: систематический скрининг на дефицит витаминов C, E, гамма-токоферола, коэнзима Q10, железа, меди, цинка, марганца, селена — все они функционируют как антиоксиданты или кофакторы антиоксидантных ферментов, и их недостаток усугубляет окислительный стресс, нарушающий фолатный метаболизм.
Перспективы: профилактика и скрининг
Данные наблюдений показывают: дети с инфантильным CFD, получившие лечение фолиновой кислотой до 2 лет, демонстрируют наилучший исход, вплоть до полного восстановления. После 6 лет прогноз существенно хуже.
При аутизме с FRα-аутоиммунитетом прогноз зависит от наличия антител у родителей:
- Антитела только у ребёнка — наиболее благоприятный ответ на терапию
- Антитела у ребёнка и одного из родителей — частичная обратимость
- Антитела у обоих родителей — неблагоприятный прогноз, несмотря на лечение
Профилактика аутизма у сиблингов
Предварительные данные трёх семей, в которых первый ребёнок страдал инфантильным аутизмом с положительными FRα-антителами:
Родители получали фолиновую кислоту в низких дозах (до 3,75 мг/сут лево-фолиновой кислоты), начиная за 3 месяца до зачатия. Матери с положительными FRα-антителами продолжали приём в течение всей беременности. Генетическое тестирование (CNV и известные гены аутизма) у первого ребёнка было нормальным.
Пять здоровых сиблингов в трёх семьях — предварительные данные, требующие подтверждения в клинических исследованиях. Но они открывают перспективу профилактического скрининга и превентивного лечения в семьях с риском.
Предложения по скринингу
Авторы обзора предлагают рассмотреть:
- Скрининг FRα-антител у матерей и в пуповинной крови
- Мониторинг ребёнка на FRα-антитела в 6, 12 и 24 месяца
- Тестирование потенциальных родителей на FRα-антитела и ассоциированные генетические варианты перед зачатием
Эти предложения требуют проведения соответствующих клинических исследований для подтверждения эффективности раннего вмешательства.
Статья подготовлена на основе обзора: Ramaekers V.T., Quadros E.V. Cerebral Folate Deficiency Syndrome: Early Diagnosis, Intervention and Treatment Strategies. Nutrients, 2022, 14, 3096.
