Когда обычные анализы не видят проблему
Представьте ситуацию: ребёнок в 4–6 месяцев стал беспокойным, плохо спит, постоянно ажитирован. Педиатр назначает стандартные анализы — общий анализ крови, фолат, B12, гомоцистеин. Всё в норме.
Но мозг этого ребёнка уже недополучает витамин B9.
Это и есть церебральный дефицит фолатов (Cerebral Folate Deficiency, CFD) — состояние, при котором уровень активной формы фолата (5-метилтетрагидрофолата, MTHF) снижен в спинномозговой жидкости, тогда как показатели крови остаются нормальными. Термин был введён в 2004 году группой исследователей под руководством Винсента Рамакерса.
Мозг и кровь разделены гематоэнцефалическим барьером. Для прохождения через него фолат нуждается в специальном рецепторе — фолатном рецепторе альфа (FRα), расположенном на клетках хориоидного сплетения. Если этот рецептор не работает — фолат остаётся в крови, а мозг голодает. И стандартный анализ крови никогда этого не покажет.
FRα-антитела: невидимый барьер
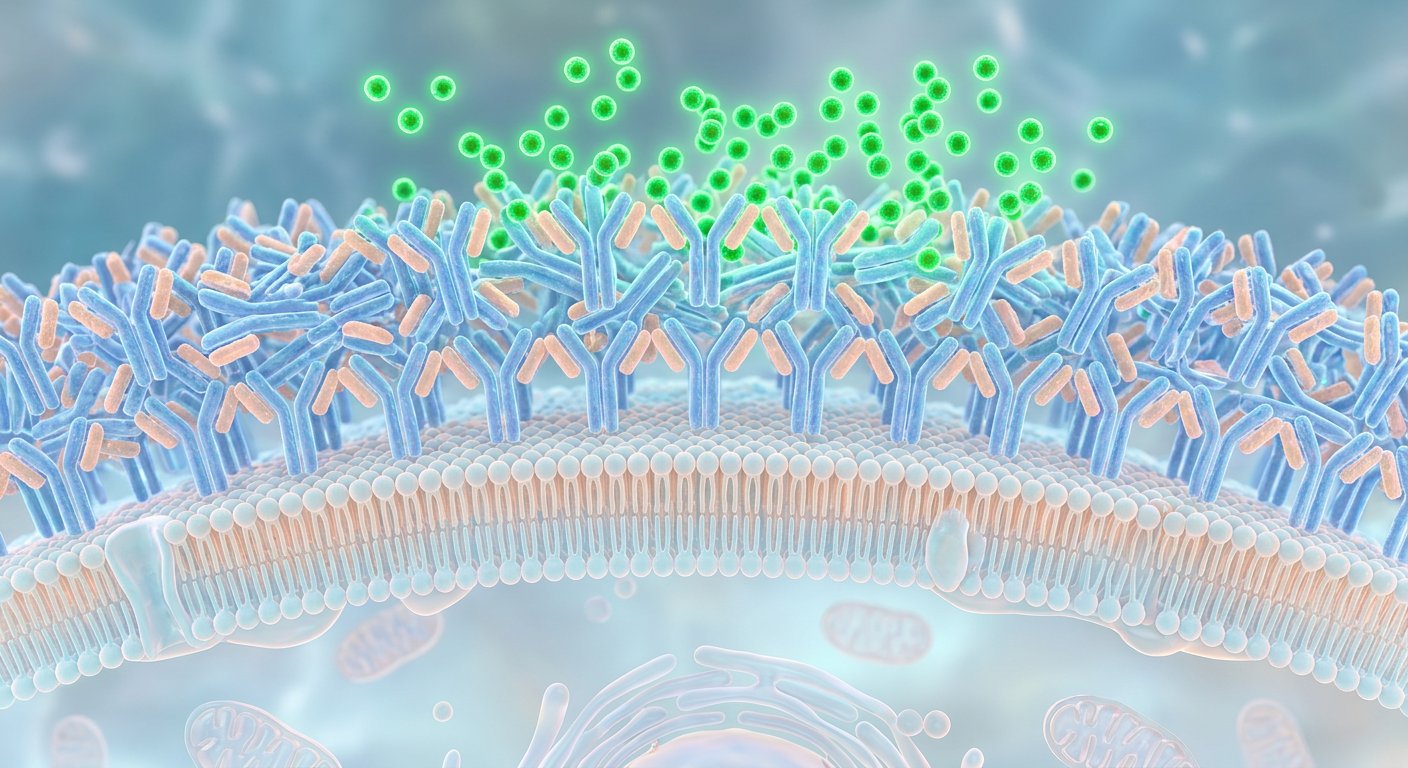
Самая распространённая причина, по которой FRα перестаёт работать, — аутоантитела. Иммунная система вырабатывает антитела, которые атакуют собственный фолатный рецептор.
Откуда они берутся? Белок FRα, присутствующий в коровьем молоке, совпадает с человеческим на 90% по аминокислотной последовательности. У генетически предрасположенных людей иммунная система начинает вырабатывать антитела против молочного FRα, а они перекрёстно реагируют с собственным рецептором на гематоэнцефалическом барьере.
Два типа антител — два механизма повреждения:
- Блокирующие — садятся прямо на участок, где фолат связывается с рецептором, и не дают витамину «пристыковаться»
- Связывающие — крепятся в другом месте, но активируют систему комплемента, которая разрушает весь комплекс
Результат один: фолат не проходит в мозг.
Доказательство механизма — простое и элегантное: безмолочная диета снижает титр FRα-антител за 3–6 месяцев. Вернуть молоко — антитела растут снова.
Ещё одна особенность: титры антител колеблются циклически с периодом 5–7 недель. Это объясняет, почему однократный отрицательный анализ не исключает диагноза — через несколько недель результат может оказаться положительным.
Возрастные окна: что искать и когда

Клиническая картина CFD определяется возрастом, в котором антитела начинают действовать. Каждому возрастному периоду соответствует свой синдром.
До рождения
Если FRα-антитела есть у матери, они нарушают транспорт фолата через плаценту. Последствия: повышенный риск дефектов нервной трубки, аутизма, задержки нейроразвития.
Если антитела есть у отца — они влияют на фолат-зависимые процессы в сперматогенезе, эпигенетическое программирование и качество ДНК.
4–6 месяцев: инфантильный CFD
Первые признаки — нарушения сна, беспокойство, ажитация, которые нельзя объяснить рефлюксом или аллергией. В течение следующих двух лет:
- Замедление роста окружности головы
- Задержка психомоторного развития, гипотония, атаксия
- Пирамидные знаки в нижних конечностях (без лечения — прогрессия до тетраспастики)
- У трети — дискинезии и судороги
- Потеря зрения с 3 лет, слуха с 6 лет
У меньшинства развивается аутизм. При МРТ у половины нелеченых — задержка миелинизации, демиелинизация, атрофия мозга и мозжечка.
Почему это окно критически важно: дети, получившие лечение фолиновой кислотой до 2 лет, показывают наилучший исход — вплоть до полного восстановления.
1–2 года: спастико-атактический синдром
Нарушения движений и обучения при появлении FRα-антител в этом возрасте.
2–5 лет: СДВГ
У части детей с синдромом дефицита внимания и гиперактивности, проблемами обучения и поведенческими отклонениями обнаруживается FRα-аутоиммунитет. Неврологически — лёгкая атаксия походки, положительная проба Ромберга.
Подростки и взрослые: психиатрический спектр
- Рефрактерная шизофрения: FRα-антитела у 85% пациентов (из 20 обследованных). Цикличность антител с периодом 5–7 недель может объяснять волнообразное течение болезни.
- Резистентная депрессия: FRα-антитела у 56% (9 из 16 пациентов).
- Дистония и паркинсонизм: спорадические случаи, не отвечающие на стандартную терапию.
Старший возраст: деменция
Описан случай деменции с миоклонусом на фоне CFD у взрослой женщины. Систематических исследований пока нет.
Лечение до 2 лет = шанс на полное восстановление

Данные наблюдений за детьми с инфантильным CFD однозначны: чем раньше начато лечение, тем лучше результат.
Дети, получившие фолиновую кислоту до 2 лет, могут полностью восстановиться — нормализация развития, исчезновение неврологических симптомов. После 6 лет прогноз значительно хуже: упущенное время — это упущенные окна нейропластичности.
Основа терапии — высокие дозы фолиновой кислоты (dl-5-формилтетрагидрофолат: 0,5–1 мг/кг/сут, при необходимости до 2 мг/кг/сут, максимум 50 мг/сут). Лево-фолиновая кислота применяется в половинных дозах.
Одно критически важное правило: начинать с половины целевой дозы. Резкое повышение фолата в мозге вызывает всплеск синтеза дофамина и серотонина. Рецепторы, которые были подавлены в условиях длительного дефицита, ещё не успели адаптироваться. Результат — выраженная ажитация и агрессия. Для установления нового равновесия нужно около 6 недель. Если ажитация выражена — временно назначается рисперидон в низкой дозе на 2–3 месяца.
Параллельно с фолиновой кислотой — безмолочная диета (замена на растительное молоко). Она убирает источник перекрёстно реагирующего FRα и снижает титр антител за 3–6 месяцев. Диету можно вводить сразу после забора диагностических образцов, не дожидаясь результатов.
Что ещё влияет на эффективность лечения
- Витамин D: его дефицит снижает экспрессию RFC1 — альтернативного транспортёра фолата. Коррекция обязательна.
- Мутации MTHFR: при C677T гомозиготном или C677T/A1298C компаунд-гетерозиготном варианте часть дозы фолиновой кислоты заменяется на лево-метил-ТГФ, плюс высокие дозы рибофлавина (B2).
- Антиоксиданты и микроэлементы: дефицит витаминов C, E, коэнзима Q10, железа, меди, цинка, марганца, селена усиливает окислительный стресс, который дополнительно разрушает фолат и FRα. Комплексная коррекция необходима.
Три семьи, пять здоровых детей
Это данные, которые могут изменить подход к планированию семьи в группах риска.
В трёх семьях первый ребёнок страдал аутизмом. У всех детей — положительные FRα-антитела. Генетическое тестирование на известные причины аутизма (CNV и ассоциированные гены) — нормальное.
Исследователи определили FRα-антитела у родителей:
Во всех трёх семьях матери были положительны. Решение: назначить обоим родителям фолиновую кислоту в низких дозах (до 3,75 мг/сут лево-фолиновой кислоты) за 3 месяца до зачатия. Матери с антителами продолжали приём в течение всей беременности.
Результат:
- Семья I: две здоровые дочери и один здоровый сын
- Семья II: одна здоровая дочь
- Семья III: один здоровый сын
Пятеро детей — все здоровы. Ни одного случая аутизма.
Пять детей — это не рандомизированное контролируемое исследование. Авторы обзора — Рамакерс и Квадрос — прямо говорят, что эти данные предварительные и требуют подтверждения в клинических исследованиях. Но они также отмечают: профилактика CFD и аутизма у потомства — «реальная возможность, если потенциальные родители будут обследованы на FRα-антитела и ассоциированные гены и получат лечение фолиновой кислотой до зачатия».
Почему прогноз зависит от антител родителей
При аутизме прогноз лечения фолиновой кислотой определяется не только сроками начала терапии, но и «антительным профилем» семьи.
Существует 8 возможных комбинаций наличия или отсутствия FRα-антител у ребёнка, матери и отца. Ключевые сценарии:
- Антитела только у ребёнка (родители отрицательны). Аутизм приобретённый — антитела появились после рождения, вероятно, под влиянием коровьего молока. Раннее лечение фолиновой кислотой и безмолочная диета дают наиболее благоприятный прогноз.
- Антитела у ребёнка и одного из родителей. Помимо постнатального дефицита фолата у ребёнка, есть воздействие на уровне гамет или внутриутробного развития. Аутизм частично обратим при лечении.
- Антитела у ребёнка и обоих родителей. Максимальное воздействие: нарушен фолат-зависимый сперматогенез, фолат-зависимое созревание ооцитов, внутриутробный транспорт фолата и постнатальный транспорт фолата в мозг. Прогноз неблагоприятный, несмотря на лечение.
Практический вывод: если после 4 месяцев терапии фолиновой кислотой у ребёнка нет значимого улучшения — нужно определить FRα-антитела у обоих родителей. Их наличие объясняет недостаточный ответ на лечение.
Что могут сделать родители и врачи сейчас
Для врачей: когда подозревать CFD
- Ребёнок 4–6 месяцев с необъяснимым беспокойством, нарушениями сна, ажитацией
- Задержка нейроразвития, замедление роста окружности головы при нормальных стандартных анализах
- Аутизм, особенно при нормальном генетическом скрининге
- СДВГ с лёгкой атаксией
- Рефрактерная шизофрения, особенно с волнообразным течением
- Терапевтически резистентная депрессия
- Дистония или паркинсонизм, не отвечающие на стандартную терапию
Первый шаг — анализ крови на FRα-аутоантитела (блокирующего и связывающего типа). Помнить о цикличности: отрицательный результат при сохраняющемся подозрении — повод для повторного тестирования через несколько недель. За 3 дня до анализа — отмена фолат-содержащих добавок.
Для семей с ребёнком с аутизмом

- Обсудить с врачом целесообразность тестирования ребёнка на FRα-антитела
- При положительном результате — тестирование обоих родителей (это влияет на прогноз)
- Генетическое консультирование перед планированием следующей беременности
Перспективы скрининга
Авторы обзора предлагают обсудить:
- Скрининг FRα-антител у беременных и в пуповинной крови
- Мониторинг ребёнка на FRα-антитела в 6, 12 и 24 месяца
- Превентивное лечение фолиновой кислотой для родителей с антителами до зачатия
Всё это пока не стандарт — но направление, которое может изменить подход к профилактике нейроразвивающих расстройств. Клинические исследования, которые подтвердят или опровергнут эти предложения, необходимы.
Статья подготовлена на основе обзора: Ramaekers V.T., Quadros E.V. Cerebral Folate Deficiency Syndrome: Early Diagnosis, Intervention and Treatment Strategies. Nutrients, 2022, 14, 3096.
